
-
医疗器械临床试验管理部门应当具备
在探讨医疗器械临床试验管理部门应当具备的关键要素时,我们不得不深入剖析这一领域所承载的复杂性与严谨性。医疗器械的临床试验,作为验证产品安全性与有效性的关键环节,不仅直接关系到患者的生命健康,也影响着医疗技术的进步与发展。因此,一个高效、专业、合规的临床试验管理部门,其构建与运营需围绕一系列核心能力与原则展开。一、专业的人员配置与团队结构首先,医疗器械临床试验管理部门应拥有一支高素质、专业化的团队。团队成员需具备深厚的医学、药学、统计学、伦理学及法规知识背景,能够全面理解并准确执行临床试验的各项要求。部门内部应明确分工,包括但不限于项目管理、数据管理、质量保证、医学监查、伦理审查等多个职能岗位,确保试验过程的每一个环节都有专人负责,且能够高效协作。二、完善的制度与流程管理制度是管理的基石,医疗···
410

-
医疗器械临床试验全过程包括哪些
医疗器械临床试验是确保医疗器械安全有效并最终获得市场准入的关键环节。这一过程涉及多个阶段和复杂步骤,从试验的初步规划到最终报告的提交,每一步都至关重要。以下是医疗器械临床试验全过程的详细阐述。一、研究设计与方案制定医疗器械临床试验的第一步是研究设计与方案制定。这一阶段的核心在于明确试验的目的、研究问题、受试者纳入和排除标准、试验组和对照组的设定、临床终点指标以及样本大小计算等。研究设计应科学合理、具有可行性,并严格遵守伦理原则。试验方案的制定需依据指导原则与产品特性,确保能够全面评估医疗器械的性能和安全性。二、伦理审查与批准在正式开展临床试验前,研究方案和相关文件需提交给当地的伦理委员会进行伦理审查。伦理委员会将评估试验的伦理合规性,确保受试者的权益得到充分保护。这一步骤是保障临床试验合法性···
280

-
医疗器械注册申报资料要求及说明
在医疗科技日新月异的今天,医疗器械作为医疗体系中的重要组成部分,其安全性、有效性和合规性直接关系到患者的生命健康与医疗质量。因此,医疗器械的注册申报过程显得尤为重要,它不仅是产品进入市场的必经之路,也是保障公众健康安全的重要环节。本文旨在详细阐述医疗器械注册申报资料的要求及说明,为相关企业及从业人员提供一份全面的指南。一、医疗器械注册申报概述医疗器械注册申报是指企业按照相关法律法规要求,向国家药品监督管理局(NMPA)或相应省级药品监督管理部门提交产品注册申请,并提供一系列证明产品安全、有效、质量可控的资料。这一过程涉及多个环节,包括产品分类界定、注册资料准备、提交审核、现场检查(如适用)、技术审评、行政审批及注册证发放等。二、医疗器械注册申报资料基本要求1. 产品基本信息产品名称:应准确、···
292

-
医疗器械咨询服务内容有哪些类型
在医疗行业的广阔领域中,医疗器械咨询服务扮演着至关重要的角色。这些服务不仅为医疗器械生产商、经销商、医疗机构及监管机构提供了全方位的支持,还促进了整个行业的健康发展。随着科技的进步和全球市场的日益融合,医疗器械咨询服务的类型和范围也在不断扩展与深化。本文将从多个维度探讨医疗器械咨询服务的具体类型及其核心价值。一、临床研究组织(CRO)服务临床研究组织是专门为医疗器械制造商提供临床试验支持的服务机构。它们的核心服务包括临床试验的设计、管理、病例招募、数据管理和监督等。CRO公司凭借丰富的临床试验经验和专业的团队,能够协助制造商高效、合规地完成临床试验,确保产品安全有效,加速上市进程。此外,CRO还负责试验数据的整理和分析,为产品注册提供坚实的数据支持。二、市场准入和注册咨询服务市场准入和注册咨···
321

-
MDSAP认证服务内容
MDSAP,即医疗器械单一审核程序(Medical Device Single Audit Program),是一项由国际医疗监管机构论坛(IMDRF)发起并推动的全球性合作项目,旨在通过一次审核,满足多个参与国家和地区对医疗器械制造商的监管要求,从而简化审核流程,降低企业成本,加速产品进入国际市场。MDSAP认证服务内容广泛而深入,涵盖了从审核准备、现场审核到后续跟踪改进的全过程,以下是该服务的详细解析。一、审核前准备1 法规符合性评估MDSAP认证服务的第一步是对企业现有质量管理体系进行全面的法规符合性评估。这包括对照MDSAP参与国(如美国FDA、加拿大Health Canada、日本MHLW/PMDA、巴西ANVISA、澳大利亚TGA等)的医疗器械法规要求,评估企业在质量管理体系、风···
385
-
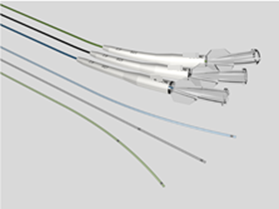
微导管NMPA注册要点
微导管NMPA注册要点一、微导管的简介微导管通常由导管管身、不透射线标记、接头等结构组成。管身通常较细且柔软,表面可带有亲水涂层。用于向血管系统中注入诊断试剂(如造影剂)、治疗试剂(如药物制剂、栓塞材料)和适当的器械(如支架、弹簧圈)等。微导管在冠状动脉粥样硬化性心脏病(冠心病)的介入治疗领域,特别是在应对极具挑战性的慢性闭塞病变(CTO)时,扮演着不可或缺且至关重要的角色。随着全球心血管疾病发病率的持续攀升,以及患者对微创手术安全性、有效性追求的日益增长,先进的导管技术成为了推动医疗进步的关键力量。微导管,凭借其超细的尺寸、卓越的灵活性和精确的操控性,完美契合了复杂冠脉介入手术的需求。它们能够轻松穿越蜿蜒曲折、狭窄甚至闭塞的血管通道,为医生提供了前所未有的治疗路径,实现了对病变部位的精准导···
564


